|
通常の有機物はよく知られているように絶縁体です.では,何故有機物は絶縁体なのでしょうか? これには大きく分けて二つの理由があります.まず一つ目はほとんどの有機分子が閉殻構造を とっており,かつHOMOとLUMOのギャップが大きいということ.二つ目は有機分子のHOMOが 分子内結合に局在化しており,分子間での軌道の重なりが非常に小さいということです. まず最初の点についてですが,HOMOとLUMOのエネルギー差が大きいということは,HOMOの 作るvalence band (VB)と,LUMOの作るconduction band (CB)とのギャップが大きいという ことを意味します. このため,通常の有機物ではVBとCBには重なりが無く,独立したバンドとなっています. ここにほとんどの有機分子が閉殻である=HOMOに2つの価電子を持つことを合わせると, VBにはバンドがちょうど埋まるだけの電子が存在し,CBには一つも電子が存在しない状態 となり,絶縁体となる事がわかります. 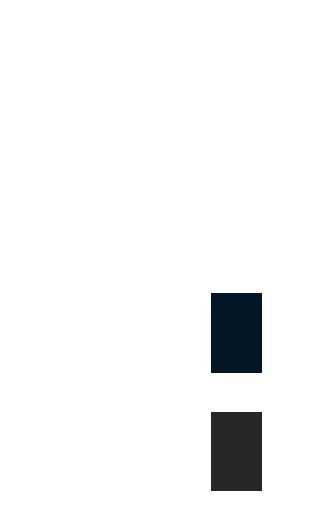 バンド形成の模式図.単分子のHOMOとLUMOからVBとCBが作られるが,両者は有機物では 重ならずに,かつ構成要素の有機分子が閉殻であるために,出来上がるバンドは空のCVと 埋まったVBになる. また,分子間での軌道の重なりが小さいということはその軌道から出来上がるバンドの幅が 狭いことを意味し,これもCBとVBが重ならないことの原因となっています. このことは逆に,これら2点を解決すれば有機分子であっても電気が流れる可能性が生まれる 事を示唆しています. まず,埋まったバンドをなんとかしなくてはなりません.このためには
代表的な分子性導体の構成分子としてTTF(ドナー)とTCNQ(アクセプタ)を例にとってみます.
TTFは分子全体に広がるπ電子系を持ち,14電子系として芳香族安定化を示します.
ここから電子を一つ取り除き酸化した場合でも,6π電子系と7π電子系の組み合わせ(両者は
入れ替わる事も可能)となり,変わらず芳香族安定化を示します.さらに環内に硫黄原子が存在し,
その非共有電子対とのカップリングによりカチオン状態でも高い安定性が確保されます.
もう一段階酸化すると二つの6π電子系となり,これもまだ安定です.
このため,TTF系分子は2段階の酸化を受けても非常に安定で,酸化状態・中性状態の間を可逆的に
移り変わることができます.  さて,このようにラジカルカチオン/アニオンを安定化できれば,対アニオン/カチオンとの塩を 作ることで空きのあるバンドを持った有機結晶を構築することが可能となります. しかしながら実はこれだけでは金属的な伝導を示す有機物は作れません. これは分子間での電子の移動がしにくい=電子の移動による安定化が少ないと,格子の歪みなどと 結びつくことで電荷を局在化させた方がエネルギーが低くなってしまうためです.特に分子性 結晶では分子間距離が比較的容易に変わるため,格子のひずみに要するエネルギーが小さくてよい ことも効いてきます. そこで,電子が移動することで得られる安定化を大きくする必要が出てきます.これにはドナーの HOMOやアクセプタのLUMO(ラジカル状態で言えばSOMO)間の重なりを大きくすることを意味します. 具体的には2分子間でのトランスファー積分(t =<Ψ1|H|Ψ2>) が大きいということになります.また一般の分子性導体では,t は重なり積分 (S =<Ψ1|Ψ2>)に比例するとおくと実験事実と 良い一致を示します. TTF系分子やTCNQなどのπ系分子はこの面でも有利で,通常の飽和結合のみからなる有機分子の HOMO(LUMO)がσ結合の位置に来てしまい分子内に局在するのに対し,π系分子ではHOMO (LUMO)が分子平面に垂直に立っています. このため,分子間で面を合わせてスタックすることでトランスファー積分を簡単に大きくすることができるわけです. さらにTTF系分子などでは分子からサイド方向に張り出した硫黄原子のd軌道なども使うことで, 横方向でも分子間の重なりを大きくし,より金属化しやすい状況となります.
さて,以上のバンド的な見方を,今度は局在的な観点から考えてみます.
電子が分子間で移動しようとするとき,まずは分子間で軌道の重なりが無ければ電子移動は
起こりません.
また,閉殻分子間での電子移動を考えると,一方の分子のHOMOの電子が,もう一方の分子の
かなりエネルギーの高いLUMOに移動しなくてはなりません.このため閉殻分子間では電子の移動は
行いにくくなります. 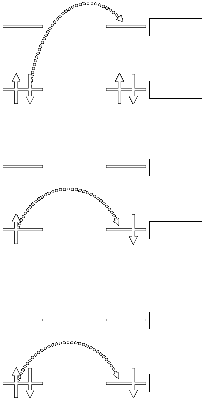
(上)閉殻分子間での電子の移動の場合,よりエネルギーの高いLUMOへ飛び移る必要があり電子は移動しにくい.
|