鉄ナノ粒子の副生成物
|
Fe@Cを合成するとき,その合成温度を240±10℃程度にし,加熱時間も12時間弱にすると, 以下の反応により副生成物として中性錯体が得られます. 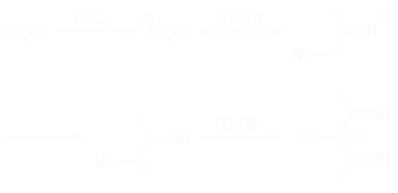
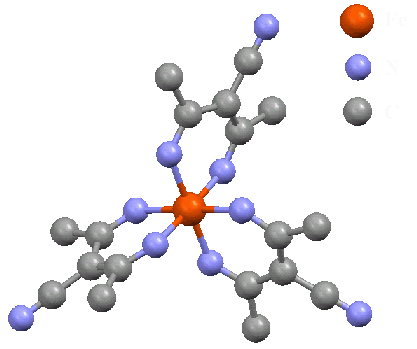
この錯体,アルコール系溶媒から再結晶により結晶化できるのですが,その結晶中に アルコール分子を取り込んでいます.そして,結晶構造はかなり溶媒分子に依存するようです. 以下に構造が解けた[FeL3]ROH (R = Me,Et)の結晶構造を示します. ![[FeL3]MeOH](C_4_3.gif) [FeL3]MeOHの結晶構造
[FeL3]MeOHでは錯体間にMeOHがはまるような形で積層しているのに対し, EtOHでは錯体が積み重なることでトンネル状の空間ができ,そこにEtOH分子が1次元に 並んだ構造となっています. *これを反映し,EtOHの方は室温近傍でも真空に引くとEtOH分子が次第に抜けてゆきます. わずかに加熱してやると急速にEtOHの脱離が進み,数十℃で完全に抜け切ります. 一方のMeOHでは錯体につかまっている分抜けにくくはなりますが,こちらも100℃を上回ったあたりで すべて抜けきります. このような構造の差は錯体間の重なりにも影響を与え,MeOHの場合は配位子間での重なりがほぼ無視できる程度になっています. 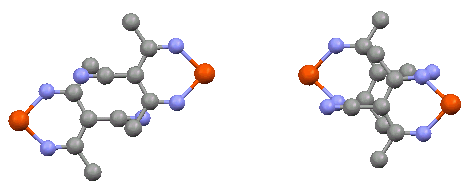 分子間での重なり.MeOHの場合(左)とEtOHの場合(右)とで大きく異なる. 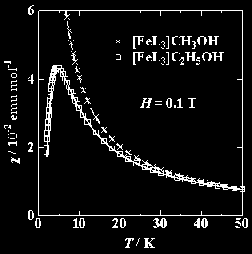 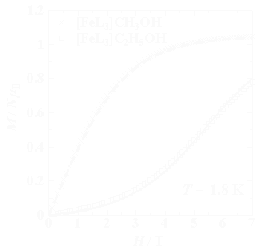
cf. J. Nishijo and N. Nishi, |
![[FeL3]EtOH](C_4_4.gif)