|
暘巕惈帴惈懱偲偼丆暥帤捠傝暘巕傪峔惉梫慺偲偟偨帴惈懱偱偡丏捠忢偺柍婡帴惈懱偑嬥懏尦慺傗偦偺巁壔暔側偳偐傜側傝慡懱偑楢懕揑偵堦懱偲側偭偰偄傞偺偵懳偟丆暘巕惈帴惈懱偱偼傑偢乽屄乆偺暘巕乿偲偄偆偒偭偪傝偲偟偨扨埵偑懚嵼偟丆偦偺暘巕偺摿挜傪斀塮偟偨僗僺儞偺僉儍儔僋僞乕偲丆僗僺儞娫亖暘巕娫偱偺憡屳嶌梡偑帴婥揑側僗僺儞攝抲傪寛掕偟傑偡丏 
偙傟偼偁傞堄枴夝愅偲偟偰偼旕忢偵妝偱偁傝丆傑偢屒棫偟偨忬懺偱偺僗僺儞偑偳偺傛偆側摿挜側偺偐丆偲偄偆偙偲偑偁傞掱搙寛掕偱偒丆師偵偦傟偑偳偺傛偆偵憡屳嶌梡偟偁偭偰偄傞偺偐傪峔憿夝愅偺僨乕僞偲撍偒崌傢偣側偑傜挷傋偰偄偔丆偲偄偆抜奒揑側夝愅偑壜擻偲側傝傑偡丏 偝偰丆偙偺傛偆側暘巕惈帴惈懱偲偟偰偼丆
 帴惈嶖懱[Cr(NCS)4Phen]-偲桳婡儔僕僇儖傾僯僆儞TCNQ- 偝偰丆偙傟傜偺暘巕惈帴惈懱偵偼丆屆揟揑側柍婡帴惈懱偲戝偒偔堎側傞惈幙偑偄偔偮偐懚嵼偟傑偡丏埲壓偵庡側摿挜傪楍婰偟偰偄偒傑偡丏 1. 暘巕偺廋忺偑壜擻嶖懱偵偣傛儔僕僇儖偵偣傛丆偦偺暘巕拞偵桳婡暘巕傪娷傓傕偺偑懡偄偨傔丆偦偙傪壔妛廋忺偡傞偙偲偱條乆側抲姺婎傪摫擖偡傞偙偲偑弌棃傑偡丏椺偊偽岝堎惈壔傪帵偡晹埵傪慻傒崬傓偙偲偱岝偵傛傞帴惈偺僗僀僢僠儞僌傪慱偭偨傝[1-2]丆儂僗僩-僎僗僩宯傪慻傓帠偱偁傞壔妛庬偑嫟懚偟偨応崌偵帴惈傪曄壔偝偣傜傟傞[3-4]丆側偳偲偄偭偨愝寁偑壜擻偲側傝傑偡丏傑偨丆攝埵巕偵抲姺婎傪偮偗傞偙偲偱暘巕娫愙怗傪惂屼偟偰丆寢徎峔憿偺惂屼亖帴婥峔憿偺惂屼傊宷偘偨椺傕抦傜傟偰偄傑偡[5]丏 偨偩偟丆偦偺愝寁偑幚嵺偵寢徎拞偱偆傑偔摥偔偐偳偆偐偵娭偟偰偼丆屻弎偺傛偆偵戝偒側栤戣偑懚嵼偟傑偡丏
懠偵傕丆揝嶖懱側偳攝埵巕応偺嫮偝偑嫮偔側傞偲掅僗僺儞偵丆媡偵庛偔側傞偲崅僗僺儞偵側傞宯偑抦傜傟偰偄傑偡丏偙偆偄偭偨宯偱偼丆椺偊偽攝埵偡傞晹暘傪巁慺偵偡傞偺偐棸墿偵偡傞偺偐傪曄偊偨傝丆攝埵巕傪彮偟廋忺偟偰旝柇側埑椡傪壛偊偨傝偡傞偙偲偱丆僗僺儞僋儘僗僆乕僶乕傪惂屼偱偒傞応崌偑偁傝傑偡[6]丏 2. 掅師尦帴惈懱偑梕堈偵峔抸偱偒傞暘巕惈帴惈懱偱偼丆懠偺暘巕偲憡屳嶌梡壜擻側億僀儞僩偑尷傜傟偰偒傑偡丏偙傟偼暘巕婳摴偑摍曽揑偱偼側偄偨傔偵丆僗僺儞枾搙偑崅偄偲偙傠乮亖憡屳嶌梡偑嫮偄偲偙傠乯傗掅偄偲偙傠乮亖摨庛偄偲偙傠乯偑惗偠偨傝丆暘巕偺宍忬偑堎曽揑偱偁傞偨傔偵椬愙暘巕偲愙怗偱偒傞偲偙傠乮亖憡屳嶌梡傪傕偰傞晹暘乯傗丆媡偵棫懱忈奞側偳偱懠偺暘巕偐傜棧傟偰偟傑偆偲偙傠乮亖憡屳嶌梡偟偵偔偄晹暘乯偑惗偠偰偔傞偨傔偱偡丏偙偺傛偆偵偛偔尷傜傟偨晹埵偱偟偐椬愙暘巕偲憡屳嶌梡弌棃側偄偨傔丆偦偺帴婥揑側僱僢僩儚乕僋偼旕忢偵堎曽揑側傕偺偲側傝偑偪偱偡丏椺偊偽暯斅忬偺暘巕偱丆柺偺忋壓偱偟偐憡屳嶌梡偑嫮偔側偄暘巕偑懚嵼偟偨偲偟傑偟傚偆丏偙偆偄偭偨暘巕摨巑偑柺傪崌傢偣偰愊傒廳側傟偽丆偱偒偁偑傞偺偼1師尦偺拰忬峔憿偱偡丏帴婥揑偵偼偙偺1師尦曽岦偱偟偐憡屳嶌梡偑婲偙傜偢丆椬愙偡傞懠偺拰偲偺娫偱偺憡屳嶌梡偼偐側傝庛偔側傞偼偢偱偡丏 偙偺応崌丆摼傜傟偨寢徎帺懱偼嶰師尦揑側偺偵丆帴婥揑偵尒傞偲傎傏1師尦丆偲偄偆暔幙偑摼傜傟傑偡丏偙偺傛偆側暔幙傪掅師尦帴惈懱偲屇傃丆暘巕惈帴惈懱偱偼媅1師尦傗媅2師尦偺帴惈懱偑旕忢偵昿斏偵摼傜傟傑偡[7-8]丏偦偆偄偭偨宯偼丆棟榑暔棟偵偍偗傞掅師尦帴惈懱偺儌僨儖暔幙偲偟偰丆棟榑偺専徹偵巊傢傟傞側偳旕忢偵嫽枴怺偄宯偲側傝傑偡丏 傕偪傠傫丆寢徎偑3師尦偱偁傞偙偲偐傜丆幚嵺偵偼旕忢偵庛偄側偑傜傕掅師尦帴惈僱僢僩儚乕僋娫偺憡屳嶌梡偑懚嵼偟丆嬌掅壏偱偼3師尦帴惈懱偲偟偰怳傞晳偄傑偡丏 暘巕惈帴惈懱偼丆偦偺懡嵤側暔幙偺峀偑傝傕娷傔丆掅師尦帴惈懱偺尋媶偺応偲偟偰偼傗偼傝堦偮敳偗弌偰偄傞揰偑偁傞傢偗偱偡丏 3. 埑椡偵傛傞暔惈惂屼偑壜擻偄傢備傞屆揟揑側柍婡帴愇偵斾傋丆暘巕惈帴惈懱偼暘巕摨巑偺僷僢僉儞僌偑娚偄偨傔丆埑椡傪偐偗傞偙偲偱暘巕娫嫍棧傪戝偒偔曄偊傞偙偲偑壜擻偱偡丏偙傟偼偮傑傝暘巕娫偱偺憡屳嶌梡偺嫮偝傪戝偒偔曄壔偝偣傜傟傞偙偲傪堄枴偟傑偡丏偙傟偵傛傝丆柍婡帴惈懱偱偼側偐側偐弌棃側偐偭偨乽憡屳嶌梡偺嫮偝傪楢懕揑偵曄壔偝偣側偑傜帴婥應掕乿偲偄偭偨偙偲偑壜擻偵側傝傑偡[9-10]丏 偝偰丆偙偙傑偱偼偳偪傜偐偲尵偊偽挿強偺晹暘偵娭偟偰弎傋偰偒傑偟偨偑丆暘巕惈帴惈懱偵偼巆擮側偑傜偙偆偄偭偨挿強傪懪偪徚偟偐偹側偄傎偳偺庛揰傕懚嵼偟偰偄傑偡丏 4. 寢徎峔憿偺惂屼偑崲擄
摿挜偺1偺偲偙傠偱乽峔憿傪惂屼偟偰塢乆乿偲彂偒傑偟偨偑丆偦偺傛偆側惂屼偑偒偪傫偲弌棃傞偙偲偼婓偱偡丏椺偊偽憌忬壔崌暔偱憌娫偵嫴傓暔傪曄偊傞丆偲偄偭偨掱搙側傜壗偲偐側傞偙偲傕懡偄乮偲偼尵偊偦傟偡傜偆傑偔偄偐側偄偙偲傕偁傞乯偺偱偡偑丆暘巕偺宍忬傪彮偟曄偊偰暘巕娫愙怗傪偪傚偭偲楳傠偆偲偟偨偩偗偱寢徎峔憿偑傑傞偭偒傝暿偺傕偺偵側偭偰偟傑偆丆側傫偰偺偼傛偔偁傞帠偱偡丏偙傟偼暘巕惈帴惈懱偺寢徎傕暘巕惈寢徎偺堦庬偱偁傝丆暘巕娫偺憡屳嶌梡偑偐側傝庛偄亖偪傚偭偲偟偨偙偲偱暿偺僷僢僉儞僌偑埨掕偵側偭偰偟傑偆偨傔偱偡丏偦偺偨傔丆寢徎峔憿傪堦偐傜愝寁偟偰乽偙傫側帴惈傪帩偨偣傛偆乿偲偄偆傛偆側偙偲偼捠忢晄壜擻偲側偭偰偟傑偄傑偡丏暘巕偺儗儀儖偱乽偙偆偄偭偨摿惈傪弌偟傗偡偄暘巕乿傪愝寁乮偙傟偼斾妑揑壜擻乯丆偦偺屻偺廤愊偺偟偐偨偼塣偵擟偣傞丆偲偄偆偺偑幚忣偵嬤偄偲偙傠丏 5. 憡屳嶌梡偑庛偄
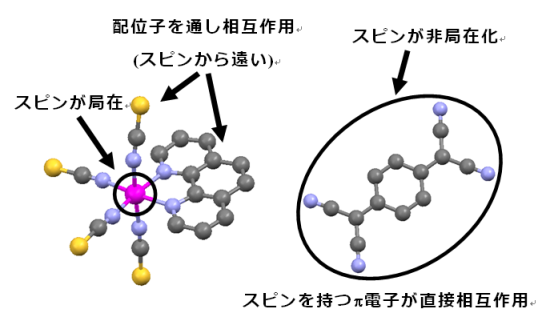
婎慴尋媶側傜傑偩偟傕丆暘巕惈帴惈懱傪壗偐偵巊偍偆偲巚偭偨嵺偵抳柦揑側寚揰偲側傞偺偑偙傟偱偡丏屆揟揑側柍婡偺帴惈懱偱偼丆椺偊偽巁壔暔偱偼僗僺儞尮摨巑偑巁慺尨巕1偮掱搙偱壦嫶偝傟偰偄傑偡丏揝扨懱側偳偱偼椬愙尨巕偑傕偆椬偺僗僺儞尮偱偡丏偙偺乽僗僺儞摨巑偺嫍棧偑嬤偄乿偲偄偆摿挜偺偨傔丆屆揟揑側帴惈懱偱偼揮堏壏搙偑幒壏偺梱偐忋丆偲偄偆傕偺偑捒偟偔偁傝傑偣傫丏 6. 抲姺偑擄偟偄傑偁丆偙傟偼昁偢偟傕抁強偲偄偆傢偗偱偼側偄偺偱偡偑乧乧丏 柍婡帴惈懱偱偼丆嬥懏尨巕傪懠偺尨巕偱抲偒姺偊偰暔惈傪僐儞僩儘乕儖偡傞丆偲偄偆偙偲偑昿斏偵峴傢傟傑偡丏崌嬥壔偟偨傝丆僼僃儔僀僩偱嬥懏傪曄偊偰暔惈傪曄偊傞傛偆側傕偺偱偡偹丏偟偐偟側偑傜暘巕惈帴惈懱偱偼丆偦傕偦傕寢徎峔憿傪婯掕偟偰偄傞憡屳嶌梡偑庛偄偨傔丆嶖懱偺拞怱嬥懏偱偁傞偲偐丆暘巕偺抲姺婎偱偁傞偲偐傪彮偟楳偭偨傕偺偲偺崿徎傪嶌傠偆偲偟偰傕偆傑偔偄偐側偄偙偲偑懡乆偁傝傑偡乮偆傑偔偄偔宯傕偁傝傑偡偑乯丏偙傟偼媡偵丆懡彮偺晄弮暔偑崿偠偭偰偄偰傕偒傟偄側寢徎偑摼傜傟傞丆偲偄偆柺偱偼僾儔僗側偺偱偡偑丆暔惈惂屼偲偄偆娤揰偐傜偼儅僀僫僗梫場偲側傝傑偡丏 偙偺傛偆偵丆暘巕惈帴惈懱偵偼屆揟揑側帴惈懱偲偼堎側傞挿強丒抁強偑懚嵼偟傑偡丏暘巕惈帴惈懱偺尋媶幰偼丆揔嵽揔強偱挿強傪巊偭偨尋媶傪偟偨傝丆壗偲偐暘巕愝寁偱抁強傪忔傝墇偊傛偆偲擔乆帋傒偰偄傞傢偗偱偡丏 丂丂
[1] S. Nakatsuji, Chem. Soc. Rev., 33 (2004) 348-353. |